AK Computer im Chemieunterricht, Vorsemester Chemie Ergänzungskurs am Gymnasium Ohmoor, Hamburg
Bestimmung der Gaskonstanten durch elektronische Druckmessung
© 14. März 1998 Carl-Jürgen Bautsch (Änderung 6.2.2007)
Zur Anwendung kommt das Programm des AK's "UNIAUS für Windows". Grundlage der Messungen bildet ein im Elektronik-Fachhandel (z.B. Fa. Conrad-Electronic) für ca. 100,-DM erwerbbarer Drucksensor von Bosch. Hier muß nur noch eine Versorgungsspannung angeschlossen werden. Ein komplettes Gerät kostet dagegen schon etwa 300,- DM. Durch eine Änderung der Größen Volumen, Temperatur und Stoffmenge können so die grundlegenden Gesetze für Gase geprüft werden. Alle drei Messreihen sind an derselben Apparatur innerhalb einer Unterrichtsstunde aufnehmbar. Die Auswertung führt schließlich zu den Gesetzen von Boyle/Mariotte, Gay/Lussac und Avogadro. Die allgemeine Gaskonstante R wird aus den Meßdaten errechnet.
Material und Versuchsdurchführung:
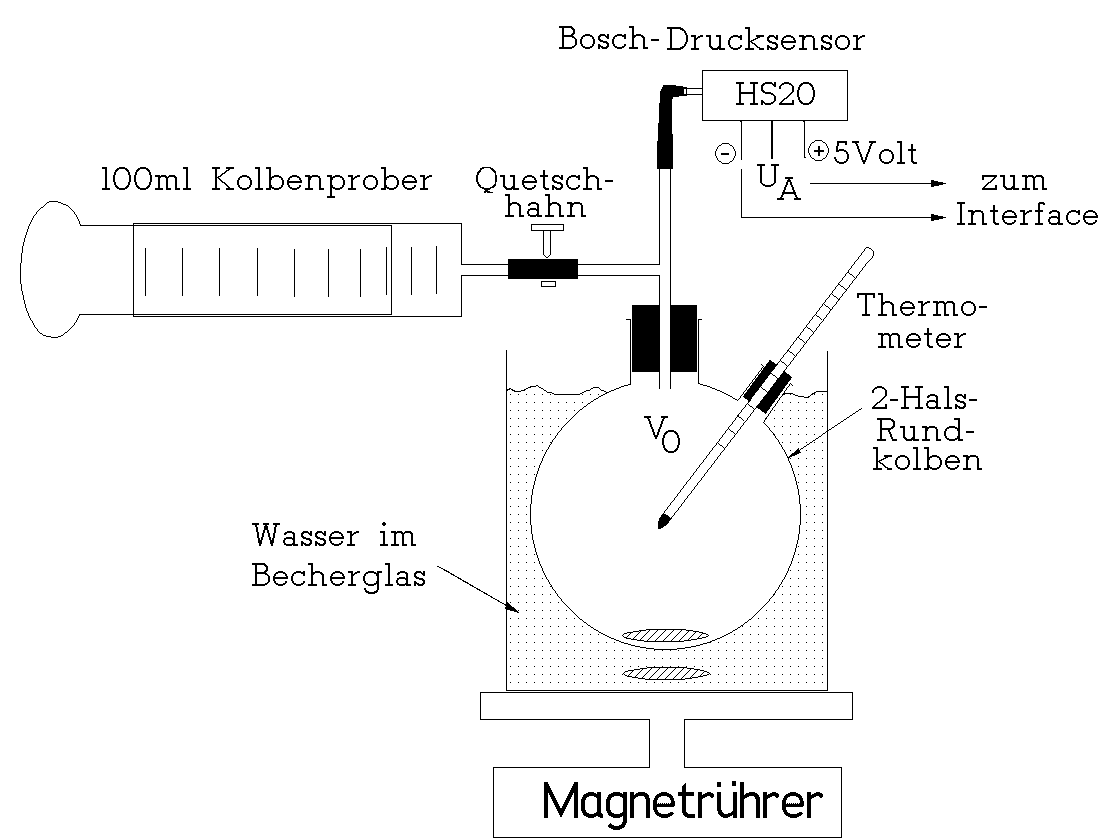
500ml 2-Halskolben, 100ml Kolbenprober, 100ml Meßzylinder, großes (1l) Becherglas, Stativ mit Klammern, Magnetrührer, Thermometer, Glasrohre, Gummischläuche, Schliffett, Experimentierkabel, Labornetzgerät, Drucksensor Bosch-HS20, 1m HCl, 8 Magnesiumstreifen mit der Masse 12 / 24 / 36 / 49 / 61 / 73 / 85 / 97 Milligram (ca. 1,5 bis 12cm)

Versuchsdurchführung: Ein 2-Halskolben wird am Stativ befestigt taucht in ein Wasser gefülltes Becherglas. Darunter befindet sich ein Magnetrührer mit Heizplatte. Sowohl in das Becherglas als auch in den Rundkolben werden Rührpillen gegeben. Über kurze Glasrohre und Gummischläuche ist das Gefäß mit einem gut gefettetem Kolbenprober sowie dem Drucksensor verbunden. Das Volumen des Kolbenprobers kann durch einen Quetschhahn vom Rundkolbeninhalt getrennt werden. In der zweiten Öffnung befindet sich ein Thermometer. Der Drucksensor ist über Experimentierkabel mit einer Gleichspannungsquelle von 5 Volt verbunden. Der Minuspol und der Ausgang werden an das Computer-Interface angeschlossen. Für die spätere Auswertung werden die Ausgangstemperatur im 2-Halskolben, der momentane Luftdruck und die Speisespannung am Sensor notiert. Das Ausgangsvolumen einschließlich der Glasrohre und Schlauchverbindungen (ohne Kolbenprober) wird schließlich noch mit Messzylindern und Wasser bestimmt.
1. Messung: Druckänderung bei Volumenzunahme Das Rührwerk ist in bewegung zu setzen. Der Kolbenprober-Stempel wird dann in Schritten von 10ml herausgezogen und die jeweilige Spannungänderung registriert. Die Volumenarbeit führt dabei zu einer geringen Abkühlung. Das umgebende Wasservolumen puffert diesen Effekt aber etwas. Unter Kontrolle der Temperatur muß zwischen den Messungen eventuell etwas gewartet werden.
2. Messung: Druckänderung bei Temperaturzunahme Das Volumen des Kolbenprobers wird mit dem Quetschhahn abgetrennt. Bei laufendem Rührwerk wird dann die Heizplatte eingeschaltet bei Anzeige von jeweils 5 Grad am Thermometer der Meßwert übernommen. Bei ca. 80 Grad Celsius wird die Meßreihe abgebrochen.
3. Messung: Druckänderung bei Zunahme der Stoffmenge Innerhalb des Kolbens sollte wieder die gleiche Temperatur, wie bei Messung 1 und 2 bestehen. In den Koben sind genau 100ml 0,1m Salzsäure zu füllen. Das Kolbenprobervolumen ist wieder angeschlossen und der Stempel wird bei 100ml arretiert. Über die Thermometeröffnung werden die vorher abgewogenen Magnesiumstreifen in die Säure gegeben. Es ist sofort wieder zu verschließen. Nachdem das Magnesium gelöst wurde und damit eine definierte Menge Wasserstoff aus der Salzsäure entwickelt hat, wird der Druckwert aufgezeichnet.
Auswertung am Computer mit UNI-AUS: Die Spannungswerte werden abgeleitet vom Beiblatt des Sensorn folgendermaßen in Druckwerte umgerechnet. UA ist dabei die aufgezeichnete Ausgangsspannung und US die Speisepannung des Sensors.
P = (39,56 * UA + 10,11) * 10 * (5/US)
Versuchsergebnisse:
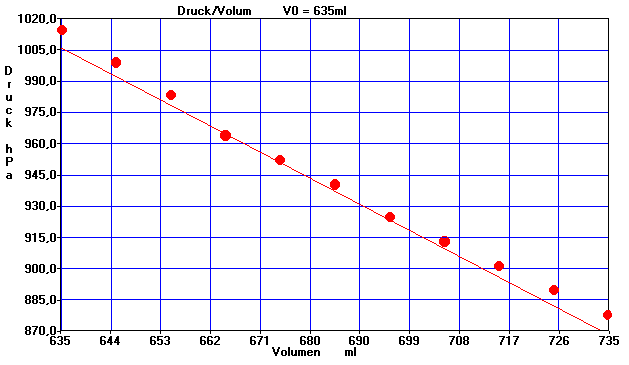
1. Druck / Volumen (Boyle / Mariotte)
Der Druck ist umgekehrt proportional zum Volumen. Es ergibt sich eine Hyperbel, deren Form hier erst durch die angelegte Tangente deutlicher hervortritt. Je nach Augangsbedingungen ergibt sich eine unterschiedliche Konstante K1, so daß der Zusammenhang lautet: P = K1 / V oder P * V = K1
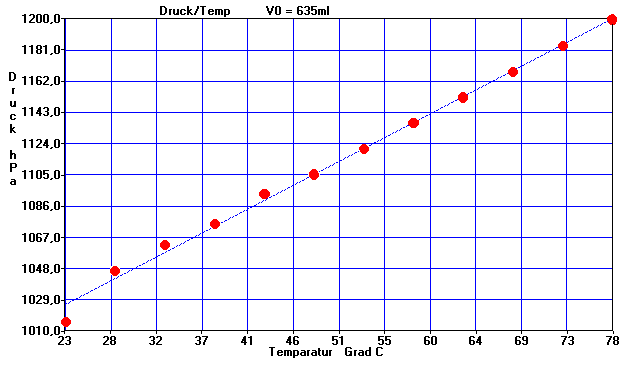
2. Druck / Temperatur (Gay-Lussac)
Der Druck (bzw. das Volumen) nimmt linear mit der Temperatur zu. Die Geradenform kann vom Programm durch eine Regression geprüft werden. Der Zusammenhang ist hier also: P = K2 * T
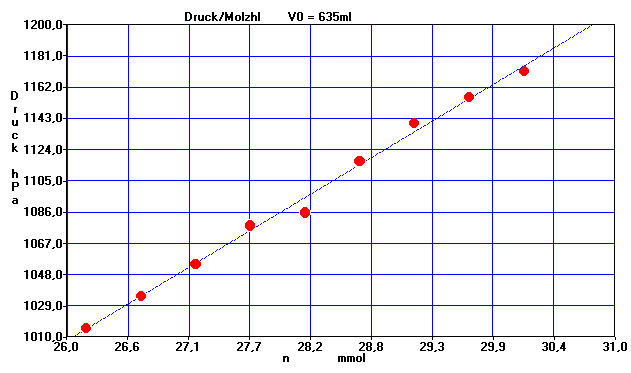
3.Druck / Stoffmenge
Der Druck (bzw. das Volumen) nimmt linear mit der Stoffmenge zu. Auch hier wurde eine Regressionsgerade berechnet. Das Gesetz lautet: P = K3 * n
Berechnung der Gaskonstanten
Alle 4 Größen hängen also über Konstanten zusammen, die in einer einzigen, der allgemeinen Gaskonstante zusammengefasst werden. Wird für Temperatur und Stoffmenge nach dem Druck umgeformt und zu einer Gleichung zusammengefasst errechnet sich R folgendermaßen: R = K1 * K2 * K3 / P0-2 [Joule / K * mol]
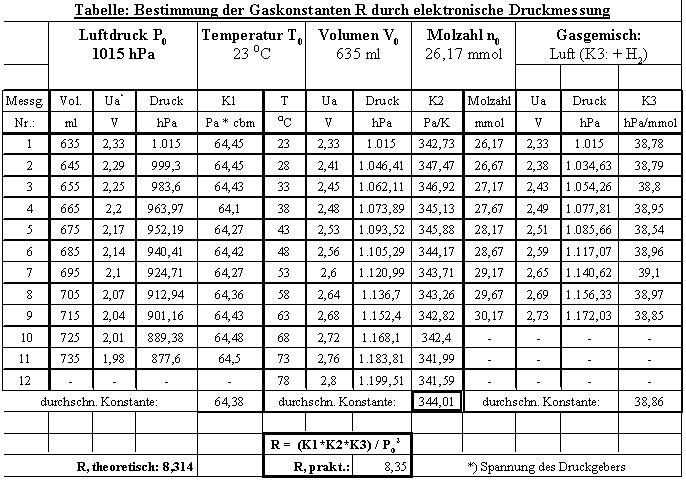
Die Tabelle zeigt die in einem Tabellenalkulationprogramm umgerechneten errechneten Konstanten K1 bis K3, deren Mittelwerte sowie die Umrechnung zu Gaskonstanten R. Es ist dabei zu beachten, dass auf gleiche Einheiten (vgl. K3!) umgerechnet werden muss. Die Abweichung vom tatsächlichen Wert 8,314 ist gering.
Kritik:
Es müsste eine Fehlerrechnung mit den Schülern durchgeführt werden. Der Drucksensor
wird nur mit einem kleinen Teil des Messbereiches ausgenutzt, entsprechend groß ist der
Fehler. Ein Vorteil wäre auch die breitere Ausnutzung des Messbereichs der Sensors. Ein
kleinerer Kolben, etwa mit nur 200ml Volumen wird eine größere Druckdynamik erzeugen und
Abweichungen so deutlicher machen.
Die Werte für V0 und P0 werden dagegen relativ gut sein. Ein Problem ist es, jedes mal die
gleichen Ausgangsbedingungen, was die Temperatur betrifft herzustellen. Das Auswiegen und
Abmessen der Magnesiumstreifen ist zeitaufwendig.